- Accueil ›
- Formation ›
- Cahiers Formation ›
- Cahiers Ordonnance ›
- La goutte
La goutte
ANALYSE D’ORDONNANCE
Le cas : Il y a quelques mois, Robert G., 61 ans, avait eu une arthrite au niveau du gros orteil gauche traitée par colchicine et son médecin lui avait fait doser son uricémie. Celle-ci s’était avérée à 110 mg/l mais, n’ayant plus de symptômes, Monsieur G., agriculteur, n’avait pas pris le temps de revoir son médecin. Ce matin, il présente à nouveau, à la suite d’un repas riche et bien arrosé, un accès douloureux à l’orteil. En sortant de consultation, il présente l’ordonnance ci-jointe.
RÉCEPTION DE L’ORDONNANCE
POUR QUI ?
Monsieur G., 61 ans.
PAR QUEL MÉDECIN ?
Dr M., son médecin traitant.
L’ORDONNANCE EST-ELLE RECEVABLE ?
Oui.
QUEL EST LE CONTEXTE DE L’ORDONNANCE ?
QUE SAVEZ-VOUS DU PATIENT ?
Robert G. est un patient connu de la pharmacie. Amateur de bonne chère et de bière, il est traité par énalapril depuis quelques années pour une hypertension artérielle, actuellement stable et équilibrée. Les différents échanges avec M. G. quand il vient chercher son antihypertenseur ont fait comprendre à l’équipe officinale que celui-ci ne respectait pas les conseils diététiques prodigués lors de sa première crise de goutte. Ses dernières analyses montrent un débit de filtration glomérulaire à 90 ml/min.
QUEL ÉTAIT LE MOTIF DE LA CONSULTATION ?
M. G. a été réveillé la nuit dernière par une douleur intense au niveau du gros orteil gauche qui est rouge et gonflé. Ayant déjà fait une crise de goutte, il a reconnu ces signes et a consulté son médecin ce matin même.
QUE LUI A DIT SON MÉDECIN ?
Compte tenu de la répétition des crises et de la valeur élevée d’uricémie, le médecin décide d’instaurer, à la suite du traitement de la crise, un traitement de fond que M. G. devra suivre à vie, en modifiant impérativement ses habitudes alimentaires.
VÉRIFICATION DE L’HISTORIQUE DU PATIENT
La consultation de l’historique révèle la dispensation régulière d’énalapril 20 mg, un inhibiteur de l’enzyme de conversion (IEC).
Le pharmacien se demande si l’inhibiteur d’enzyme de conversion ne contribue pas à augmenter l’uricémie de M. G. et si son traitement antihypertenseur ne devrait pas être réévalué : en effet, le losartan (aux propriétés hypo-uricémiantes) et les inhibiteurs calciques (qui ne sont pas hyperuricémiants) paraissent mieux adaptés pour traiter l’hypertension artérielle d’un patient goutteux. Equipé d’une messagerie sécurisée de santé, le pharmacien décide, avec l’accord de M. G., d’envoyer un message au médecin traitant, pour en discuter avec lui. En attendant l’avis du médecin, M. G. doit continuer à prendre correctement l’énalapril.LA PRESCRIPTION EST-ELLE COHÉRENTE ?
QUE COMPORTE LA PRESCRIPTION ?
La colchicine est un alcaloïde antigoutteux et anti-inflammatoire, qui empêche la précipitation des cristaux d’urate.
L’allopurinol (Zyloric) est un inhibiteur de la xanthine oxydase. Il inhibe la synthèse d’acide urique et exerce donc un effet hypo-uricémiant.EST-ELLE CONFORME À LA STRATÉGIE THÉRAPEUTIQUE ?
Oui. Le traitement de l’accès goutteux doit être instauré le plus tôt possible. Le médecin prescrit à cet effet de la colchicine pour soulager rapidement les symptômes de la crise.
Les dernières recommandations de l’Eular de 2016 favorisent la mise en place d’un traitement de fond dès le premier accès pour obtenir la dissolution des cristaux d’urate et éviter les récidives. Le traitement hypo-uricémiant n’avait pas encore été instauré, car M. G., très pris par son exploitation agricole, n’avait pas reconsulté avec ses résultats d’uricémie. D’après les recommandations de l’Eular, l’allopurinol est l’hypo-uricémiant de première intention chez le sujet normorénal.
Le traitement de fond doit être débuté à distance d’une crise aiguë, associé à de la colchicine à dose prophylactique (pendant en général 6 mois après obtention de l’uricémie cible) afin de prévenir le risque de crises fréquentes en début de traitement hypo-uricémiant.Y A-T-IL DES MÉDICAMENTS À MARGE THÉRAPEUTIQUE ÉTROITE ?
Oui, la colchicine a une marge thérapeutique étroite.
Y A-T-IL DES CONTRE-INDICATIONS POUR CE PATIENT ?
M. G. ne souffrant pas d’insuffisance rénale ou hépatique sévère, la prise de colchicine n’est pas contre-indiquée. Le patient prend pour la première fois de l’allopurinol. Il n’a donc pas d’antécédent de toxidermie à cette molécule qui contre-indiquerait sa prise.
LES POSOLOGIES SONT-ELLES COHÉRENTES ?
En traitement de la crise, la colchicine est prescrite à doses dégressives. Selon les dernières recommandations de l’Eular, la posologie de colchicine tend à diminuer afin d’améliorer la tolérance digestive (le premier jour, 1 mg en dose de charge, suivie, 1 heure plus tard, d’1/2 cp, éventuellement à renouveler sans dépasser 2 mg/j, puis 1,5 mg au maximum les jours suivants). Un relais à 0,5 mg sans interruption de traitement vise à éviter tout risque de nouvelle crise de goutte, dans l’attente de l’initiation du traitement de fond, 2 semaines au minimum après la résolution de la crise. Il est à continuer pendant quelques mois après initiation du traitement de fond.
La posologie initiale d’allopurinol est conforme au résumé des caractéristiques du produit (RCP). Si au bout de 1 à 2 mois, l’objectif uricémique n’est pas atteint, la posologie pourra être progressivement augmentée jusqu’à éventuellement 300 mg par jour, compte tenu de la fonction rénale du patient.Y A-T-IL DES INTERACTIONS ?
Non.
LE TRAITEMENT NÉCESSITE-T-IL UNE SURVEILLANCE PARTICULIÈRE ?
Il est recommandé de contrôler la numération de formule sanguine afin de rechercher une éventuelle hématoxicité liée à la colchicine et de surveiller la fonction rénale.
Sous allopurinol, il est également recommandé de surveiller la fonction rénale.QUELS CONSEILS DE PRISE DONNER ?
QUAND COMMENCER LE TRAITEMENT ?
M. G. doit débuter la colchicine sans attendre. Elle est plus efficace quand elle est administrée précocement.
Le traitement de fond sera débuté à distance de la crise (au moins 2 semaines après sa résolution).INTERVENTION PHARMACEUTIQUE
M. G. s’étonne de voir que le pharmacien a déposé sur le comptoir 2 boîtes de Colchicine Opocalcium : « La dernière fois, une seule boîte m’a suffi, il me reste même des comprimés ! ».
Il est important de bien expliquer le schéma posologique au patient. Le médecin lui a prescrit de la colchicine. Cette fois, contrairement à la crise précédente, le patient doit poursuivre le traitement à une dose plus faible après la cessation de la crise. Quinze jours après résolution de la crise, la colchicine sera associée au traitement de fond hypo-uricémiant qui, dans les premiers mois, peut être à l’origine de crises de goutte. Elles ne signifient pas que l’allopurinol est inefficace. Il faudra donc rassurer le patient et l’inciter à continuer son traitement.QUE FAIRE EN CAS D’OUBLI ?
En cas d’oubli de prise de l’allopurinol, ne pas doubler la dose lors de la prochaine prise, la demi-vie de l’oxypurinol, le métabolite actif de l’allopurinol, étant de 20 heures.
LE PATIENT POURRA-T-IL JUGER DE L’EFFICACITÉ DU TRAITEMENT ?
La colchicine va rapidement soulager la douleur. L’apparition de crises de goutte, malgré la prise des traitements, n’est pas un signe d’inefficacité et ne doit en aucun cas faire arrêter le traitement. La crise est provoquée par la diminution rapide de l’uricémie.
QUELS SONT LES PRINCIPAUX EFFETS INDÉSIRABLES ?
Des troubles gastro-intestinaux sont assez fréquents (nausées, vomissements, diarrhées) avec la colchicine et le fébuxostat.
Des anomalies hématologiques et des toxidermies (rares mais potentiellement graves) peuvent s’observer avec l’allopurinol.QUELS SIGNES NÉCESSITERAIENT D’APPELER LE MÉDECIN ?
La survenue de diarrhées constitue l’un des premiers signes d’un surdosage en colchicine. Elles doivent être signalées au médecin en vue d’une réévaluation du traitement, ainsi que la survenue d’éruptions cutanées ou d’atteintes muqueuses sous allopurinol.
CONSEILS COMPLÉMENTAIRES
Insister sur l’observance du traitement de fond, il s’agit d’un traitement au long cours qui ne doit pas être interrompu. Réexpliquer à M. G. que le dosage de l’uricémie permet de s’assurer de l’efficacité du traitement et que l’objectif est d’abaisser l’uricémie en dessous de 60 mg/l.
Réexpliquer le plan de prise de la colchicine.
Réitérer les conseils hygiénodiététiques qui, jusqu’à présent, n’ont pas été suivis : pratiquer une activité physique régulière (excepté pendant la crise), encourager une réduction pondérale, boire environ 2 litres d’eau par jour, proscrire les alcools forts et la bière, limiter la consommation de viandes rouges, d’abats, de charcuterie, de gibier, de certains poissons (sardines, harengs, anchois, etc.) et de fruits de mer, privilégier les fruits et légumes et les laitages maigres (à potentiel uricosurique).
Eduquer le patient à signaler la prise de ce traitement en cas de nouvelle consultation médicale (risque d’interactions avec la colchicine) et à bannir l’automédication par aspirine ou ibuprofène en raison du traitement par énalapril (risque d’insuffisance rénale aiguë).
Insister sur la surveillance indispensable de son uricémie, de sa clairance rénale et de sa pression artérielle.
Uricémie
Taux d’acide urique dans le sang. Les normales d’uricémie sont :
Chez l’homme : 35-70 mg/l (ou 210 à 420 μmol/l)
Chez la femme : 25-60 mg/l (ou 150 à 360 μmol/l)
Objectif uricémique
L’objectif du traitement de fond hypo-uricémiant sera d’abaisser l’uricémie en dessous de 60 mg/l.
EULAR
European league against rheumatism, Organisationreprésentant les personnes souffrant d’arthrite et/ou de rhumatismes, les professionnels de santé et les sociétés scientifiques de rhumatologie de toutes les nations européennes.Par Solange Loizon et Maïtena Teknetzian , pharmaciennes, avec la collaboration du D r Jérôme Gillard , rhumatologue, Centre hospitalier Jura Sud, site Lons le Saunier.
PATHOLOGIE
Depuis toujours assimilée à la maladie des princes et des rois car elle touchait des hommes à l’alimentation trop riche et alcoolisée, la goutte, dont la fréquence a doublé chez les femmes ces 20 dernières années, constitue actuellement l’arthropathie inflammatoire la plus fréquente en Occident.
1 QU’EST-CE QUE C’EST ?
La goutte est la principale représentante des arthropathies microcristallines. Conséquence d’une hyperuricémie chronique, c’est une maladie rhumatismale inflammatoire, évoluant par poussées appelées « accès goutteux » ou « crises de goutte », dues à la présence de cristaux d’urate dans les articulations.
Sans traitement correctement mené, les crises de goutte se répètent à une fréquence variable.
2 QUELS SONT LES SIGNES CLINIQUES ?
DE LA CRISE DE GOUTTE
La crise peut être précédée de prodromes (asthénie, insomnie, irritabilité ou anorexie).
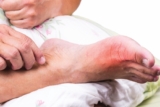
Elle est caractérisée par une douleur intense et brutale. Le plus nocturne, elle empêche le sommeil. La localisation la plus typique est l’articulation métatarsophalangienne du gros orteil mais toutes les articulations peuvent être concernées. L’articulation est rouge, gonflée et chaude. Cette inflammation importante peut s’accompagner de fièvre. Sans traitement, la crise est spontanément résolutive en quelques jours (jusqu’à 2 semaines).
Après un épisode aigu, la peau de la zone concernée desquame. A la fin de la crise, l’articulation retrouve son aspect normal.PublicitéDE LA GOUTTE CHRONIQUE
Entre 2 épisodes aigus, la maladie est silencieuse mais les taux d’acide urique restent élevés et les cristaux s’accumulent.
Après quelques années d’hyperuricémie, 3 signes majeurs peuvent être identifiés :
– une atteinte polyarticulaire avec des articulations déformées, tuméfiées, douloureuses et raides ;
– l’apparition de tophi autour des articulations mais aussi sous la peau au niveau des coudes, des mains, des tendons d’Achille ou du pavillon de l’oreille ;
– des manifestations rénales (lithiases uriques, néphropathie voire insuffisance rénale chronique).3 COMMENT EST POSÉ LE DIAGNOSTIC ?
La localisation de l’inflammation et les symptômes de la crise sont caractéristiques et orientent le diagnostic.
Lors d’un accès aigu, un syndrome inflammatoire (augmentation de la vitesse de sédimentation et de la protéine C réactive, hyperleucocytose) est observé. L’uricémie est dans certains cas normale au cours de l’accès goutteux (effet uricosurique des interleukines libérées pendant la crise).
L’examen du liquide articulaire montre un aspect trouble et la présence de nombreuses cellules polynucléaires (confirmant l’arthrite) et révèle la présence de cristaux allongés et effilés d’urate de sodium (confirmant l’étiologie goutteuse). Ces cristaux peuvent être retrouvés même en dehors des crises, dans le cas où l’articulation a déjà été douloureuse précédemment. L’échographie peut être une alternative à la ponction.
Le score de Nijmegen a aussi un intérêt en médecine générale pour orienter le diagnostic, si la ponction articulaire n’est pas possible.
La radiographie sera peu utile au stade aigu mais significative en cas de goutte chronique pour observer une destruction articulaire.4 AVEC QUELLES PATHOLOGIES NE PAS LA CONFONDRE ?
La crise aiguë ne doit pas être confondue avec le rhumatisme psoriasique qui peut se manifester initialement par un orteil « en saucisse de cocktail ».
Les autres diagnostics différentiels sont représentés par les autres arthropathies microcristallines : la chondrocalcinose (à cristaux de pyrophosphate de calcium) et le rhumatisme à cristaux d’hydroxyapatite, ce dernier affectant le plus souvent l’épaule.
En cas de fièvre élevée et d’élévation majeure de la protéine C réactive, si la ponction articulaire découvre un liquide stérile en culture, cela permet d’exclure l’arthrite septique.5 QUELS SONT LES ÉTIOLOGIES ET FACTEURS PRÉDISPOSANTS ?
DE LA GOUTTE PRIMITIVE
La prévalence de la goutte augmente avec l’âge.
La prédominance de la maladie est largement masculine mais cet écart entre hommes et femmes diminue avec l’âge. La prévalence augmente chez la femme ménopausée (rôle uricosurique des œstrogènes).
Un excès d’apport en purines (viande, crustacés, abats, sardines, harengs, bière, etc.) favorise l’hyperuricémie. Le fructose présent dans les sodas sucrés favorise aussi la production d’urates.
Le facteur génétique est clairement identifiable. 40 % des goutteux ont un parent goutteux. Certaines mutations de gènes, codant pour des protéines transportrices au niveau tubulaire, expliquent en effet des défauts d’excrétion rénale de l’acide urique.
La goutte congénitale ou syndrome de Lesch-Nyhan est rare (< 1/200 000 naissances).DE LA GOUTTE SECONDAIRE
La cause la plus fréquente de goutte secondaire est iatrogène. Les médicaments impliqués sont les diurétiques thiazidiques et de l’anse, mais aussi l’aspirine à faible dose, les immunosuppresseurs (ciclosporine, tacrolimus) et certains antituberculeux (pyrazinamide, ethambutol) ou antiviraux (ritonavir, lopinavir, didanosine, interférons pégylés).
Des pathologies peuvent aussi être à l’origine de goutte : insuffisance rénale chronique, mais aussi certaines hémopathies malignes et pathologies tumorales en raison d’un syndrome de lyse à l’origine d’une hyperuricémie consécutive aux chimiothérapies anticancéreuses.
Le syndrome métabolique (associant hypertension artérielle, dyslipidémie, obésité et hyperglycémie) serait un facteur de risque prédisposant à la goutte.6 QUELLES COMPLICATIONS ?
En l’absence de traitement ou de respect des mesures hygiénodiététiques, les principales complications sont d’ordre rénal et articulaire. Au niveau rénal, les dépôts de cristaux peuvent être à l’origine de lithiases et de crises de coliques néphrétiques. La complication majeure est l’insuffisance rénale chronique.
Au niveau articulaire, l’accumulation des tophi engendre des douleurs et des difficultés motrices et fonctionnelles liées à la destruction progressive des articulations touchées.
Enfin, un lien entre hyperuricémie et augmentation du risque cardiovasculaire semble établi bien que toutes les études ne s’accordent pas sur la nature de ce lien, à savoir si l’hyperuricémie est une cause ou une conséquence de l’hypertension artérielle.
Tophi (pluriel de tophus)
Nodule ferme, indolore et blanchâtre correspondant à un amas composé de cristaux d’urate de sodium.
Score de NIJMEGEN
Modèle prédictif intégrant le sexe masculin, la récidive au moins 1 fois d’un accès, la survenue de l’arthrite en moins de 24 heures, la rougeur, l’atteinte de la première articulation métatarso-phalangienne, une HTA ou maladie cardiovasculaire et une uricémie > 60 mg/l.
PurineS
Molécules azotées entrant dans la constitution des nucléotides, précurseurs de l’acide urique.
Inflamma-some
Complexe pro-inflammatoire activant la cyclo-oxygénase de type 2, l’interleukine 1β et 8 et le tumor necrosis factor alpha (TNF α).Par Bérangère Balaj Leroy et Maïtena Teknetzian , pharmaciennes, avec la collaboration du D r Jean-Louis Paul , rhumatologue à Metz.
THÉRAPEUTIQUE
Le traitement de la goutte s’est amélioré depuis quelques années grâce une meilleure connaissance de sa physiopathologie. Il combine médicaments indiqués dans l’accès aigu et d’autres abaissant l’uricémie.
STRATÉGIE THÉRAPEUTIQUE
OBJECTIFS DU TRAITEMENT
La stratégie thérapeutique repose sur un traitement de la crise aiguë qui limite les douleurs et le handicap, mais aussi sur un traitement de fond, mis en place dès le premier accès pour limiter le risque de récidive et en cas de formation de tophus, d’arthropathie uratique et de calculs rénaux (recommandations européennes, Eular 2016).
L’objectif du traitement de fond est d’abaisser l’uricémie en dessous de 60 mg/l (ou 360 µmol/l) voire 50 mg/l (300 µmol/l). Le choix des différentes molécules dépend des contre-indications et des comorbidités du patient.
Le traitement de la goutte nécessite aussi des mesures diététiques, une prise en charge pluridisciplinaire et, dans la mesure du possible, l’éducation thérapeutique du patient pour le faire adhérer à un traitement à vie.
La prise en charge concomitante des comorbidités associées, à savoir obésité, insuffisance rénale chronique, dyslipidémie, diabète, hypertension artérielle (HTA), maladies cardiovasculaires, psoriasis et syndrome d’apnées du sommeil, est essentielle.
TRAITEMENT DE L’ACCÈS AIGU
Le traitement doit être mis en place précocement (dans les 12 heures). Il associe repos articulaire et traitements symptomatiques.
EN PREMIÈRE INTENTION
Precrits en monothérapie ou associés, la colchicine et les anti-inflammatoires non stéroïdiens (AINS) sont proposés en première intention. Le choix est effectué en fonction de l’âge du patient et des comorbidités digestives, rénales et cardiovasculaires. L’aspirine ne doit pas être utilisée car elle interfère avec l’élimination urinaire de l’acide urique.
EN DEUXIÈME INTENTION
En cas d’échec ou de contre-indication aux AINS et à la colchicine, il est possible d’utiliser des corticoïdes per os et en cures courtes. Ils sont à éviter chez le diabétique. Après avoir écarté une atteinte infectieuse de l’articulation, il est possible de réaliser une injection intra-articulaire lorsque l’atteinte est isolée.
Le canakinumab (inhibiteur de l’interleukine 1) n’est prescrit que chez des patients adultes présentant des crises fréquentes (au moins 3 crises au cours des 12 derniers mois), dans les formes de goutte sévères résistantes ou lorsqu’il y a des contre-indications aux autres traitements. Sa prescription induit un surrisque infectieux et il est nécessaire de réaliser un bilan infectieux (tuberculose, hépatite, etc.) avant la première injection.TRAITEMENT DE FOND
Un traitement hypo-uricémiant doit être envisagé à la première crise dès que le diagnostic de goutte est confirmé (hyperuricémie symptomatique : crise de goutte, arthropathie, tophus ou lithiase). Il est d’autant plus nécessaire que le patient est jeune (< 40 ans) ou avec des comorbidités. En traitant précocement, il est possible de dissoudre les cristaux d’urates.
Le traitement hypo-uricémiant doit débuter au minimum 1 à 2 semaines après la fin de l’accès goutteux pour avoir une évaluation correcte de l’uricémie (effet uricosurique de l’inflammation).EN PREMIÈRE INTENTION
Les inhibiteurs de la xanthine oxydase (allopurinol, fébuxostat) sont recommandés en première intention.
Les recommandations de l’Eular 2016, tenant compte de l’efficacité, du coût et de la sécurité, placent l’allopurinol en première ligne et le fébuxostat en seconde ligne en cas d’antécédent de toxidermies sous allopurinol, d’inefficacité de celui-ci ou en cas d’insuffisance rénale. En effet, son excrétion mixte (et minoritaire par voie rénale) en fait une alternative intéressante dans ce cas. Mais, en juin 2019, l’ANSM a alerté sur les risques accrus, chez les patients traités par fébuxostat, de mortalité en cas d’antécédents de maladies cardiovasculaires majeures.
Pour éviter un accès goutteux, un traitement par colchicine (0,5 à 1 mg par jour) ou, en l’absence de diabète, par corticoïdes (5 à 10 mg d’équivalent prednisone par jour) doit être instauré en prophylaxie pendant 6 mois. En pratique, les spécialistes évitent l’usage prophylactique des AINS (risque d’effets digestifs, néphrotoxiques et d’interactions).EN DEUXIÈME INTENTION
En cas d’échec, il est possible de recourir en deuxième intention à un médicament uricosurique (probénécide, inhibiteur de la réabsorption tubulaire de l’acide urique) associé aux inhibiteurs de xanthine oxydase ou utilisé seul s’il y a intolérance ou contre-indication à ceux-ci.
TRAITEMENT DES COMORBIDITÉS
Certains traitements peuvent augmenter l’uricémie. C’est pourquoi il est préférable de privilégier le clopidogrel à l’aspirine et d’utiliser préférentiellement comme diurétique la spironolactone. Le losartan, certains antagonistes calciques, le fénofibrate et l’atorvastatine ont un effet hypo-uricémiant. Les biguanides doivent être privilégiés dans le diabète.
TRAITEMENTS
DE L’ACCÈS
REPOS ET GLAÇAGE
Le repos articulaire pendant 1 à 2 jours permettrait de diminuer la durée de prise des médicaments. L’application de glace pendant au moins 15 minutes 2 à 3 fois par jour réduit la douleur et limite le gonflement.
LA COLCHICINE
La colchicine réduit l’activation de l’inflammasome.
Elle doit être administrée le plus précocement possible, et ce, jusqu’à la disparition des signes locaux. Ainsi, il est recommandé que le patient ait quelques comprimés d’avance. Son effet se manifeste 10 à 24 heures après le début du traitement et la douleur régresse dans la plupart des cas en 3 à 4 jours.
Chez le sujet âgé, il faut adapter les doses en fonction de la clairance de la créatinine (ClCr) : 0,5 mg 2 fois par jour si ClCr > 50 ml/min, 0,5 mg par jour si ClCr entre 35 et 49 ml/min. En cas d’insuffisance rénale sévère, il est possible d’administrer 0,5 mg tous les 2 à 3 jours si la clairance est comprise entre 10 et 34 ml/min.
Effets indésirables : les diarrhées représentent un des premiers signes d’un surdosage en colchicine. Dans Colchimax, la poudre d’opium et le tiémonium limitent cet effet et les douleurs intestinales qui l’accompagnent. Cependant, la présence systématique d’un antidiarrhéique n’est pas toujours conseillée (car il peut masquer les signes de surdosage) sauf si une petite dose de colchicine reste mal tolérée. Des nausées et vomissements sont également fréquents. Des troubles neurologiques et une toxicité hématologique peuvent apparaître plus rarement.
Interactions : les macrolides (sauf spiramycine) et la pristinamycine sont contre-indiqués avec la colchicine car ils diminuent son métabolisme entraînant un surdosage potentiellement fatal.
L’association avec les inhibiteurs de la P-glycoprotéine (P-gp) et du cytochrome P450 3A4 (ciclosporine, vérapamil, antifongiques azolés, inhibiteur des protéases boostées par ritonavir, etc.) est déconseillée.
L’association de la colchicine avec les statines fait l’objet de précautions d’emploi (risque de rhabdomyolyse). Il en est de même lors de l’association avec un antivitamine K (AVK), avec une augmentation du risque hémorragique. Eviter la consommation de jus de pamplemousse.LES AINS
Les AINS présentent une activité anti-inflammatoire, antalgique et antipyrétique. Indométacine et kétoprofène ont une AMM dans le traitement de la crise de goutte, l’ibuprofène et le diclofénac dans les arthropathies microcristallines. Cependant, toutes les molécules sont utilisables dans la crise de goutte.
Les AINS auraient une rapidité d’action supérieure à la colchicine, ainsi douleur et sensibilité s’améliorent significativement à partir du 4e jour. En monothérapie, le choix entre AINS et colchicine doit tenir compte de la fonction rénale et des comorbidités cardiovasculaires du patient.
Effets indésirables : les troubles digestifs, les réactions d’hypersensibilité (manifestations cutanées parfois sévères, bronchospasme) ou les troubles neuropsychiques (vertiges, céphalées) représentent les principaux effets indésirables. Le piroxicam est associé à un risque élevé de toxidermies sévères et de manifestations digestives graves. Les AINS induisent un risque infectieux. Ils augmentent le temps de saignement et favorisent la survenue d’insuffisance rénale fonctionnelle. L’usage d’AINS au long cours expose à un risque cardiovasculaire (notamment le diclofénac). Le naproxène semblerait mieux toléré au niveau cardiovasculaire chez le patient jeune.
Interactions : leur association avec des anticoagulants est déconseillée (risque d’hémorragies). L’association au méthotrexate à des doses supérieures à 20 mg par semaine est déconseillée (majoration de sa toxicité hématologique). L’association avec des médicaments antihypertenseurs, notamment diurétiques, inhibiteurs de l’enzyme de conversion et antagonistes des récepteurs à l’angiotensine 2, fait l’objet de précautions d’emploi (risque d’insuffisance rénale aiguë chez les patients âgés et/ou déshydratés).LES CORTICOÏDES
30 à 35 mg d’équivalent prednisone sont utilisés pendant 5 à 10 jours. La durée de traitement doit être limitée dans le temps pour éviter une résistance au traitement (« goutte cortisonée »). Le traitement, court et à faibles doses, provoque peu d’effets secondaires mais des perturbations métaboliques sont possibles chez le diabétique et l’hypertendu.
Interactions : l’association aux vaccins vivants est contre-indiquée (risque de maladie vaccinale généralisée).LE CANAKINUMAB
Le canakinumab est efficace sur la douleur mais aussi sur le risque de récidive d’une crise dans les 12 semaines suivant le traitement. C’est un immunosuppresseur inhibiteur de l’interleukine 1 qui empêche la synthèse de médiateurs de l’inflammation.
Il faut l’injecter en 1 seule dose de 150 mg par voie sous-cutanée dès le début de la crise pour optimiser l’efficacité. Les sites d’injection sont les hauts des bras et des cuisses, les fesses et l’abdomen. En cas de récidive d’une crise, il faut attendre 12 semaines pour une nouvelle injection. En cas d’échec de la première injection, il est inutile de renouveler le traitement.
Effets indésirables : le risque infectieux (infections respiratoires, mycoses vaginales) représente l’effet indésirable principal. Des réactions au site d’injection, des douleurs abdominales, des arthralgies et de la fatigue sont fréquentes. Une diminution de la clairance rénale et des perturbations des lignées sanguines peuvent s’observer.
Interactions : l’association à un anti-TNF αest déconseillée. Le canakinumab étant inhibiteur enzymatique, il faut être prudent avec les médicaments substrats des cytochromes P450.DE FOND (HYPO-URICÉMIANT)
L’ALLOPURINOL
Il représente le traitement de première ligne. Il inhibe la xanthine oxydase et est métabolisé en oxypurinol qui est lui aussi inhibiteur de la xanthine oxydase.
Effets indésirables : l’allopurinol peut provoquer des toxidermies rares mais potentiellement fatales, pendant les 3 premiers mois de traitement le plus souvent. La survenue d’une éruption cutanée ou de signes d’hypersensibilité (atteinte des yeux, de la bouche, des muqueuses génitales, fièvre, adénopathie) impose son arrêt. La reprise d’allopurinol est alors formellement contre-indiquée. Le risque de survenue de toxidermies sévères semble plus fréquent chez les patients porteurs de l’allèle HLA B*5801 (porté le plus souvent par des sujets asiatiques). Compte tenu de la faible prévalence de cet allèle en Europe, les recommandations de l’Eular ne préconisent pas son dépistage systématique avant initiation du traitement. Quelques rares cas de troubles digestifs peuvent également apparaître.
Interactions : l’association de l’allopurinol aux antipurines (aziathioprine, mercaptopurine) est contre-indiquée (risque d’insuffisance médullaire).
Il doit être utilisé avec précautions avec les AVK (perturbation de l’INR), avec les pénicillines (augmentation de la toxicité cutanée) et le furosémide (augmentation de l’uricémie).LE FÉBUXOSTAT
Inhibiteur sélectif de la xanthine oxydase, il est intéressant en cas d’inefficacité, d’intolérance ou de contre-indication à l’allopurinol. Contrairement à ce dernier, éliminé majoritairement par voie rénale, le fébuxostat est éliminé par voies rénale et hépatique (pas d’ajustement posologique en fonction de la clairance).
Effets indésirables : diarrhées, nausées, céphalées, œdèmes et complications cardiovasculaires potentiellement létales représentent les effets secondaires les plus fréquents. Le fébuxostat peut perturber la fonction hépatique (nécessité d’un bilan hépatique avant la mise sous traitement puis de façon périodique) et provoquer des toxidermies graves (toute éruption ou signe d’hypersensibilité doit être signalé) non croisées avec l’allopurinol. Des troubles musculosquelettiques (arthrite, arthralgie, myalgie, faiblesse musculaire, etc.) sont possibles. Les rhabdomyolyses sont rares.
Interactions : le fébuxostat est contre-indiqué avec les antipurines.Les uricosuriques
Actuellement et de façon temporaire, seul Probenecid Biokanol est disponible en pharmacie hospitalière. Il est réservé à des patients sans insuffisance rénale ni hyperuraturie ni lithiase urinaire.
Interactions : le probénécide est contre-indiqué avec le méthotrexate (diminution de l’excrétion rénale de ce dernier et majoration de sa toxicité). Il est déconseillé avec les pénicillines et l’aspirine car il en augmente les concentrations plasmatiques par diminution de la sécrétion rénale tubulaire.PERSPECTIVES
Le lésinurad (Zurampic) est un uricosurique qui, en association avec l’allopurinol, permettrait d’abaisser l’uricémie. La spécialité est en attente de prix.
Le pegloticase a une AMM européenne mais n’est pas disponible en France. Cette molécule, grâce à ses propriétés d’uricase, réduirait massivement des dépôts d’urates dans les gouttes sévères.
Un nouvel inhibiteur de la xanthine oxydase (topiroxostat) est commercialisé au Japon.
Uricase
Enzyme qui catalyse la conversion de l’acide urique plasmatique en allantoïne, composé soluble éliminé par excrétion rénale. La diminution de l’acide urique sérique permet la formation d’un gradient de concentration entre les cristaux d’urates de l’articulation et l’acide urique sérique ce qui favorise la dissolution des cristaux.
Par Stéphanie Satger , pharmacienne, avec la collaboration du P r Gérard Chalès , professeur émérite de rhumatologie à la faculté de Médecine de Rennes, rhumatologue au CHU de Rennes.
ACCOMPAGNER LE PATIENT
« En juin 2016 à l’occasion d’une exploration d’un pied douloureux, le radiologue a fortement suggéré le diagnostic de goutte. J’ai eu des dosages mensuels d’acide urique tous inférieurs à 50 mg/l. Dix-huit mois plus tard, quelques jours après une hospitalisation pour des problèmes urologiques, j’ai eu mon premier accès de goutte, après un dîner accompagné d’un verre de bière. Le médecin m’a prescrit de la colchicine pour soigner l’épisode aigu puis, après disparition de la crise douloureuse, a lancé un traitement par allopurinol. Mon uricémie était alors à 58 mg/l. Le traitement contrôle relativement bien la pathologie malgré de fréquentes « douleurs en aiguille ». Je suis beaucoup plus vigilant sur mes apports alimentaires. Je diminue les rations caloriques et me limite à des viandes blanches, du jambon, du poisson avec des fruits et légumes. »
LA GOUTTE VUE PAR LE PATIENT
IMPACT SUR LA VIE QUOTIDIENNE
En cas de crise, la douleur est très vive et difficile à supporter. Tout contact avec l’articulation douloureuse (même celle d’un vêtement ou d’un drap) peut devenir insupportable. Ces exacerbations se manifestant typiquement la nuit, la qualité du sommeil est altérée si un traitement efficace n’est pas mis en place.
Au niveau professionnel, les douleurs peuvent diminuer les capacités physiques du patient et justifier un arrêt de travail ponctuel.
En outre, les effets secondaires digestifs de la colchicine peuvent gêner le patient au quotidien. Les AINS peuvent provoquer des gastralgies parfois mal supportées par les patients.IMPACT PSYCHOLOGIQUE
En cas de traitement de fond, le fait de devoir prendre un traitement chronique peut avoir un effet sur le moral du patient, surtout en cas d’efficacité retardée.
La nécessaire adaptation du régime alimentaire est souvent vécue comme une contrainte car les concessions sont synonymes de privation et peuvent impacter les repas pris au restaurant ou chez des amis.À DIRE AU PATIENT
A PROPOS DE LA MALADIE
ACTIVITÉ PHYSIQUE
La goutte étant une pathologie articulaire, les patients peuvent être tentés à tort de supprimer toute activité physique, pensant que la mise au repos est nécessaire. Il convient de leur rappeler qu’une activité physique douce et modérée, comme la marche rapide, le vélo ou la natation, est bénéfique et contribue à lutter contre la surcharge pondérale.
Cependant, lors d’un accès aigu, l’articulation douloureuse doit être mise au repos, notamment lorsque le poignet est concerné. Des orthèses d’immobilisation peuvent être utilisées à cet effet.ADAPTATION DE L’ALIMENTATION
Boire 1,5 à 2 litres d’eau par jour. Le café et le thé sont autorisés (éviter le thé vert cependant). Le vin est à consommer avec modération (2 verres par jour). Les alcools forts et la bière (même sans alcool) sont à éviter impérativement, de même que les boissons riches en fructose.
Les viandes blanches (sans la peau des volailles, riche en purines, et à raison de 100 à 120 g par jour, poids de la portion cuite), le jambon maigre (80 g par jour) ou les œufs (mode de cuisson sans graisse) seront préférés à la viande rouge, aux abats et à la charcuterie. Le poisson sera consommé 2 fois par semaine. Les crustacés et les fruits de mer sont à éviter.
Consommer des laitages en privilégiant ceux à teneur réduite en matière grasse.
Légumes verts et céréales sont permis sans restriction, les fruits peuvent être consommés 2 à 3 fois par jour.EN CAS DE CRISE
En plus des traitements symptomatiques, les crises de goutte peuvent être soulagées par l’application d’une poche de glace sur l’articulation (3 fois par jour pendant plusieurs minutes). Pour éviter les brûlures par le froid, la poche sera appliquée avec un linge pour protéger la peau.
A PROPOS DES TRAITEMENTS
ADHÉSION THÉRAPEUTIQUE
La goutte étant une pathologie chronique, son traitement nécessite une bonne adhésion au traitement même si les crises sont très espacées ou inexistantes. Expliquer au patient que si le traitement est interrompu, l’uricémie remonte et les crises réapparaissent après quelques mois voire en quelques semaines.
Expliquer au patient la distinction entre le traitement de l’accès aigu (symptomatique et ponctuel) et celui de l’hyperuricémie (traitement de fond au long cours, permettant de diminuer la fréquence et l’intensité des crises et de prévenir les complications). Ce dernier est à poursuivre aussi bien en l’absence d’accès qu’en période de crises.
S’assurer que le schéma de prise de colchicine en cas de crise est bien connu par le patient et qu’il en dispose toujours sur lui. Une mise en œuvre rapide de ce traitement (moins de 12 heures après le début) permet d’obtenir une efficacité maximale à posologie moindre.GESTION DES EFFETS INDÉSIRABLES
Conseiller de prendre les AINS au cours des repas pour limiter les gastralgies potentielles.
En cas de diarrhées sous colchicine, penser à une possibilité de surdosage et orienter le patient vers son médecin en vue d’une réévaluation du traitement (réduction des posologies voire suspension). Informer le patient que de nombreux médicaments sont susceptibles d’interagir avec la colchicine et de modifier la réponse au traitement et déconseiller l’automédication.
En cas de survenue d’éruption cutanée sous allopurinol, orienter impérativement le patient vers une consultation médicale rapide.SUIVI
Le dosage de l’uricémie est utilisé comme guide de suivi de traitement : l’objectif est de maintenir une uricémie inférieure à 60 mg/l.
La surveillance de la fonction rénale est nécessaire, notamment pour adapter les posologies de colchicine et d’allopurinol et déceler d’éventuelles complications.
Un bilan hépatique est à réaliser avant instauration d’un traitement par fébuxostat et régulièrement par la suite.
La goutte s’inscrivant dans un contexte de comorbidités et de polypathologies, il est important de contrôler régulièrement la tension artérielle, la glycémie et la lipidémie.
Par Bérangère Balaj Leroy avec la collaboration du Dr Jean-Louis Paul , rhumatologue à Metz.
DÉLIVRERIEZ-VOUS CES ORDONNANCES ?
LE TRAITEMENT EST-IL CONFORME À LA STRATÉGIE THÉRAPEUTIQUE ?
– Traitement de crise : la posologie de colchicine a été revue à la baisse en 2016 : le premier jour, dose de charge de 1 mg, suivie 1 heure plus tard d’une dose de 0,5 mg (jusqu’à 2 mg par jour au maximum) puis 1 à 1,5 mg par jour ensuite.
– Traitement de fond : un traitement hypo-uricémiant (allopurinol en première ligne) doit être envisagé dès la première crise, 2 semaines après sa résolution. Il est associé, pendant environ 6 mois généralement, à un traitement prophylactique par colchicine à faible dose (de l’ordre de 0,5 mg par jour).L’ORDONNANCE EST-ELLE RECEVABLE ?
Le canakinumab (Ilaris) est soumis à prescription hospitalière, réservée à certains spécialistes.
Y A-T-IL DES INTERACTIONS ?
Outre les interactions impliquant les AINS, être particulièrement attentif aux interactions avec la colchicine (à marge thérapeutique étroite) : elle est contre-indiquée avec les macrolides (sauf spiramycine) et lapristinamycine et déconseillée avec les autres inhibiteurs enzymatiques.
LE PATIENT CONNAÎT-IL L’OBJECTIF THÉRAPEUTIQUE ?
L’objectif est d’abaisser l’uricémie en dessous de 60 mg/l voire 50 mg/l.
L’HYPERURICÉMIE PEUT-ELLE ÊTRE D’ORIGINE IATROGÈNE ?
S’interroger sur une éventuelle origine iatrogène en cas de délivrance de diurétiques de l’anse ou thiazidiques, de bêtabloquants, d’inhibiteurs de l’enzyme de conversion (IEC) ou d’antagonistes des récepteurs de l’angiotensine II (ARA II), autres que losartan, pour envisager avec le prescripteur une réévaluation du traitement (le losartan et les inhibiteurs calciques sont uricosuriques).
LE PATIENT EST-IL CORRECTEMENT SURVEILLÉ ?
Outre l’uricémie et le suivi biologique relatif aux effets indésirables (NFS, bilan hépatique), s’assurer du contrôle régulier de la fonction rénale.
En raison d’un risque accru d’événements cardiovasculaires graves sous fébuxostat, inciter les patients ayant des antécédents cardiovasculaires à consulter leur médecin.QUELS CONSEILS DONNER ?
– Hygiénodiététiques : proscrire les alcools forts, la bière même sans alcool et les boissons riches en fructose, limiter la consommation de viandes rouges et de charcuterie, avoir une alimentation équilibrée riche en fruits et légumes (les purines d’origine végétale sont sans incidence sur la goutte).
– En cas de crise : mettre l’articulation douloureuse au repos et appliquer de la glace.
– En cas d’effets indésirables : orienter vers le médecin en cas de diarrhées sous colchicine, de réaction cutanée sous allopurinol ou de douleurs musculaires sous fébuxostat.Art1_46-Encadre-SousEncadreA-Image_E5.jpg
Cahiers Ordonnance
- Pathologie
- Stratégie thérapeutique
- Traitements
- Analyse d’ordonnance
- Conseils associés
- Bibliographie
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
- Stratégie thérapeutique
Des questions sur les tests de lecture et la validation de votre DPC ?
formation@lemoniteurdespharmacies.fr
Tél : 06 49 72 16 11


Dénutrition des séniors à l’officine
Roger, l’ancien titulaire, passe régulièrement vous voir. Vous remarquez qu’il maigrit et marche difficilement. Comment aborder ce sujet délicat et dépister une dénutrition chez votre patient âgé ?

Anxiété et dépression à l’officine
Anita, jeune maman, pleure sans raison depuis l’accouchement. Son médecin diagnostique une dépression et prescrit citalopram et zolpidem. Elle pensait au baby blues et hésite à prendre ces médicaments…

Tabac : Engagez-vous en prévention santé
Lucie, 25 ans, veut un bébé, mais fume 12 cigarettes/jour. Patchs, gommes, acupuncture… elle est perdue. Quels conseils lui donner pour un sevrage réussi ? Accompagnez-la efficacement.
Cancer de la prostate
Maurice, 65 ans, sous hormonothérapie pour un cancer de la prostate, reçoit son bon vaccin grippe. Mais peut-il se faire vacciner avec son traitement ? Saurez-vous le rassurer et le conseiller ?