- Accueil ›
- Thérapeutique ›
- Médicaments ›
- Fiches médicaments ›
- Dans le traitement de l’hépatite C
Dans le traitement de l’hépatite C
A base de sofosbuvir, Sovaldi est un traitement oral pangénotypique de l’hépatite C chronique, c’est-à-dire actif sur tous les génotypes du virus de l’hépatite C. Il doit toujours être utilisé en association.
INDICATION
Sovaldi est indiqué en association à d’autres médicaments pour le traitement de l’hépatite C chronique chez les adultes et les adolescents âgés de 12 ans à moins de 18 ans.
POSOLOGIE
La dose recommandée est d’un comprimé dosé à 400 mg une fois par jour, par voie orale, avec de la nourriture.
La durée du traitement varie de 12 à 24 semaines selon le génotype et les médicaments associés (ribavirine +/- peginterféron alfa). Elle peut être augmentée pour les patients en attente de transplantation hépatique.
Sovaldi peut être utilisé chez les adolescents atteints d’une hépatite chronique de génotype 2 ou 3.
En cas d’oubli constaté dans les 18 heures suivant la prise habituelle, le comprimé doit être pris le plus tôt possible, et la dose suivante comme prévu. Si l’oubli est constaté plus de 18 heures après, la dose sera omise et le patient prendra la dose suivante comme prévu sans la doubler.
CONTRE-INDICATIONS
Hypersensibilité au sofosbuvir ou à un excipient.
Utilisation avec des inducteurs puissants de la glycoprotéine P (P-gp) dans l’intestin (rifampicine, rifabutine, millepertuis, carbamazépine, phénobarbital, phénytoïne), en raison du risque de diminution de la concentration de sofosbuvir et d’une perte d’efficacité.
Prudence en cas de conduite de véhicule ou d’utilisation de machines, la prise de sofosbuvir pouvant provoquer des troubles de l’attention, des sensations vertigineuses et de la fatigue.
GROSSESSE ET ALLAITEMENT
Par mesure de précaution, l’utilisation de Sovaldi pendant la grossesse doit être évitée.
Sovaldi ne doit pas être utilisé pendant l’allaitement.
Des effets tératogènes et/ou embryocides ont été démontrés chez toutes les espèces animales exposées à la ribavirine. Les femmes traitées en âge de procréer doivent utiliser une méthode de contraception efficace au cours du traitement et pendant 4 mois après l’arrêt de la ribavirine. Les hommes traités et leurs partenaires féminines doivent utiliser une contraception jusqu’à 7 mois après l’arrêt de la ribavirine.
EFFETS INDÉSIRABLES
Les effets indésirables les plus fréquents survenus chez les patients sous sofosbuvir et ribavirine +/- peginterféron alfa ont été la fatigue, les maux de tête, les nausées et l’insomnie.
Très fréquemment ont aussi été décrits des anomalies sanguines (diminution de l’hémoglobine, anémie, neutropénie, lymphopénie, thrombopénie), des sensations vertigineuses, des vomissements, une diarrhée, une dyspnée, une toux, une augmentation de la bilirubine sérique, un rash, un prurit, des arthralgies, des myalgies, des frissons, un syndrome pseudogrippal, de l’irritabilité.
INTERACTIONS MÉDICAMENTEUSES
Association aux puissants inducteurs de la P-gp contre-indiquée (voir paragraphe Contre-indications).
Association aux inducteurs modérés de la P-gp intestinale (oxcarbazépine, modafinil) déconseillée.
Des cas de bradycardie sévère et de troubles de la conduction ont été observés avec le sofosbuvir en association avec un autre antiviral d’action directe (dont le lédipasvir, in Harvoni), lors de la co-administration avec l’amiodarone et/ou d’autres médicaments diminuant la fréquence cardiaque.
– Avaler le comprimé en entier. Ne pas le croquer ni l’écraser, en raison du goût amer du sofosbuvir.
– En cas de vomissement dans les 2 heures suivant la prise, un autre comprimé doit être pris. Au-delà de 2 heures, il n’est pas nécessaire de prendre un autre comprimé.
– La fonction hépatique pouvant changer au cours du traitement par Sovaldi, une surveillance étroite de l’INR s’impose pour les patients traités par antagonistes de la vitamine K.
Sofosbuvir 400 mg, comprimé pelliculé, flacon de 28, avec fermeture de sécurité enfant, avec du Silicagel comme déshydratant et un tampon de polyester, 9 897,70 €, remb. SS à 100 %, AMM : 34009 277 070 7 0
Gilead Sciences : 01 46 09 41 00
Les prix sont mentionnés hors honoraires de dispensation.
– Service médical rendu important
– Amélioration du service médical rendu importante (ASMR II) pour l’ensemble des patients adultes infectés par le VHC (excepté les patients de génotype 3 naïfs de traitement antiviral), modérée (ASMR III) pour les patients adultes infectés par un VHC de génotype 3 naïfs de traitement antiviral
– Population cible estimée à 130 000 patients
• Liste I
• Prescription hospitalière
• Prescription réservée aux spécialistes en gastro-entérologie et hépatologie, en médecine interne ou en infectiologie
En France, près de 200 000 personnes seraient atteintes par une infection chronique du virus de l’hépatite C.
Qu’est-ce que c’est ?
L’hépatite C est une maladie virale dont la transmission se fait essentiellement par voie sanguine. Le mode de contamination le plus fréquent est la toxicomanie intraveineuse et nasale, les autres voies de transmission (sexuelle, materno-fœtale lors de l’accouchement ou l’exposition accidentelle au sang) étant plus rares. En dehors de ces comportements, différents facteurs de risque sont identifiés : pays d’origine à forte prévalence du virus de l’hépatite C, infection par le VIH et précarité sociale. L’infection aiguë, le plus souvent asymptomatique, évolue soit vers une guérison spontanée dans un délai de six mois (15 à 35 % des cas), soit vers la chronicité (65 à 85 % des cas).
L’infection chronique se manifeste par des symptômes : – hépatiques allant de la fibrose à la cirrhose, avec un risque de cirrhose compris entre 15 et 30 % après 20 ans d’évolution de la maladie ; – extrahépatiques (fatigue, syndrome sec…).
Quels sont les différents génotypes du VHC ?
Le virus de l’hépatite C, dont le génome est un ARN, présente une grande variabilité génétique. Les fréquences des 7 génotypes majeurs identifiés varient en fonction de la localisation géographique. En France, les génotypes 1a et 1b sont les plus fréquents, représentant 61 % des cas. Le génotype 3 qui concerne 19 % des patients en France est associé à un risque plus élevé de cirrhose et de carcinome hépatocellulaire. Les autres génotypes, 2 (9 %), 4, (9 %), 5 (2 %) et 6 (moins de 1 %) sont plus rares en France.
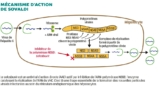
1 COMMENT AGIT LE MÉDICAMENT ?
Le sofosbuvir (Sovaldi) est un inhibiteur pangénotypique de l’ARN polymérase ARN-dépendante NS5B du virus de l’hépatite C (VHC), essentielle à sa réplication.
Il s’agit de la prodrogue d’un nucléotide qui subit une métabolisation intracellulaire pour former un analogue de l’uridine triphosphate qui peut être incorporé dans l’ARN viral par la polymérase NS5B et agit comme « terminateur » de chaîne, bloquant donc son élongation.2 SON ACTION EST-ELLE ORIGINALE ?
Elle l’était à l’époque de la commercialisation hospitalière du sofosbuvir. D’autres anti-VHC partagent depuis son mode d’action, comme le dasabuvir (Exviera à l’hôpital).
Le sofosbuvir est également commercialisé en association fixe à un inhibiteur NS5A : le lédipasvir (Harvoni) ou le velpatasvir (Epclusa).3 QUEL EST LE VERDICT DES ÉTUDES CLINIQUES ?
L’efficacité et la tolérance du sofosbuvir ont été évaluées par la Haute Autorité de santé (mai 2014) dans 5 études cliniques de phase III chez des patients infectés par un VHC de génotype 1 à 6 ayant une maladie hépatique compensée, notamment une cirrhose. Il a été administré à la dose de 400 mg/j, avec une dose de ribavirine calculée en fonction du poids (1000-1200 mg/j en 2 doses fractionnées) ; la dose de peginterferon alfa2a était, si besoin, de 180 µg/semaine.
Une étude de phase III non comparative (étude NEUTRINO) a évalué l’efficacité d’un traitement de 12 semaines par sofosbuvir + peginterféron alfa 2a + ribavirine chez 327 sujets infectés par un VHC de génotype 1, 4, 5 et 6 naïfs de traitement. Le pourcentage de réponse virologique a été de 90,5 % (tous génotypes confondus) et d’environ 80 % chez les sujets cirrhotiques.
Une bithérapie sofosbuvir + ribavirine sur 24 semaines s’est révélée efficace avec un pourcentage de réponse virale soutenue 12 semaines après la fin du traitement (RVS12), compris entre 50 % et 76 % selon les études (QUANTUM et PHOTON-1).
Pour les patients infectés par un génotype 2, une bithérapie de 12 semaines sofosbuvir + ribavirine a donné des pourcentages de RVS12 de 97 % chez les sujets naïfs (versus 78 % avec un traitement de 24 semaines par bithérapie peginterféron alfa 2a + ribavirine) -étude FISSION- et de 93 % chez les sujets inéligibles, intolérants ou refusant l’IFN (étude POSITRON).
Pour les patients infectés par un génotype 3, une bithérapie de 24 semaines sofosbuvir + ribavirine (étude VALENCE) a donné des pourcentages de RVS12 de 93 % chez les sujets naïfs et de 77 % chez les patients prétraités (l’efficacité moins importante vis-à-vis du génotype 3 explique la nécessité de 24 semaines de traitement au lieu de 12 pour le génotype 2).
Aucun cas de résistance n’a été observé chez les patients traités par sofosbuvir dans les études de phase III.
Denis Richard
- Comptoir officinal : optimiser l’espace sans sacrifier la relation patient
- Reishi, shiitaké, maitaké : la poussée des champignons médicinaux
- Budget de la sécu 2026 : quelles mesures concernent les pharmaciens ?
- Cancers féminins : des voies de traitements prometteuses
- Vitamine A Blache 15 000 UI/g : un remplaçant pour Vitamine A Dulcis